Investigadores del CIBERCV han identificado el papel clave de las enzimas lisil oxidasa (LOX) y lisil hidroxilasa 1 (PLOD1) en los procesos de calcificación vascular. El estudio, publicado en la revista The FASEB Journal, apunta a estas dos enzimas como potenciales dianas terapéuticas hacia las que dirigir nuevas estrategias de control farmacológico para limitar este proceso.
En la última década, diversos estudios epidemiológicos han determinado que la calcificación vascular es un factor pronóstico independiente de mortalidad cardiovascular y una de las principales características de las lesiones ateroscleróticas avanzadas.
Relación entre la formación ósea y la calcificación vascular
Las enzimas lisil oxidasa y lisil hidroxilasa 1 participan en la síntesis y maduración del colágeno de matriz extracelular. La matriz extracelular (ECM, por sus siglas en inglés) está implicada en la comunicación y la diferenciación celular y ejerce una gran cantidad de funciones biológicas, entre las que figura su contribución al proceso de formación del tejido óseo (osteogénesis). Curiosamente, la osteogénesis fisiológica comparte similitudes con la mineralización ectópica patológica, incluida la calcificación vascular.
En este nuevo estudio, desarrollado por los grupos de investigación del CIBERCV que lideran Francisco Marín en el Instituto Murciano de Investigación Biosanitaria Virgen de la Arrixaca (IMIB-Arrixaca) y José Martínez-González en el CSIC -Institut de Recerca Hospital de la Santa Creu i Sant Pau, se evaluó la contribución de estas enzimas durante la calcificación inducida por hiperfosfatemia de la célula de músculo liso vascular (CMLV).
Los investigadores observaron que, durante la calcificación vascular, las células del músculo liso vascular (CMLV) se diferencian en células similares a los osteoblastos (células implicadas de la formación ósea), lo que induce una remodelación activa y una calcificación de la matriz extracelular.
Los datos de este estudio demostraron que las enzimas involucradas en el ensamblaje adecuado del colágeno participan en esta mineralización ectópica promoviendo la transdiferenciación de las células del músculo liso vascular en células similares a los osteoblastos.
Para obtener estos resultados, los investigadores emplearon estrategias de inhibición farmacológica de estas enzimas en células vasculares humanas y de ratón y animales modificados genéticamente. “Hemos demostrado el impacto potencial de la inhibición de LOX y PLOD en la prevención de la calcificación vascular”, concluyen las investigadoras principales del estudio, Cristina Rodríguez (Institut de Recerca Hospital de la Santa Creu i Sant Pau) y Diana Hernández-Romero (Instituto Murciano de Investigación Sanitaria Virgen de la Arrixaca, IMIB-Arrixaca).
Artículo de referencia:
Inhibition of enzymes involved in collagen cross-linking reduces vascular smooth muscle cell calcification. Jover E, Silvente A, Marín F, Martínez-González J, Orriols M, Martínez CM, Puche CM, Valdés M, Rodríguez C, Hernández-Romero D. FASEB J. 2018 Mar 16:fj201700653R. DOI: 10.1096/fj.201700653R
Figura:
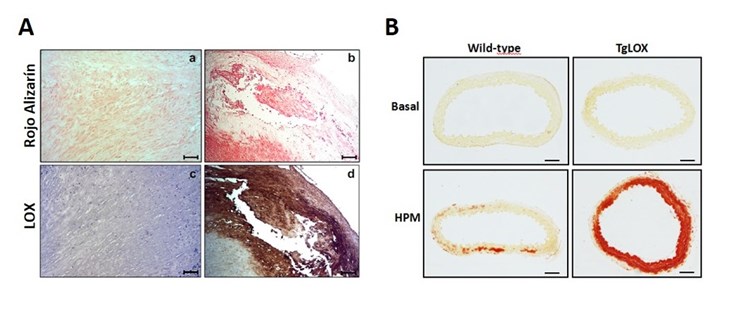
LOX se expresa en lesiones ateroscleróticas humanas y su sobreexpresión en ratón promueve la mineralización vascular. A) Secciones representativas de arteria femoral de pacientes sometidos a cirugía cardíaca. En las muestras negativas para la tinción de Rojo Alizarín para calcificación residual (a) la expresión de LOX es negligible (c), mientras las lesiones calcificadas (b) presentan una fuerte inmunotinción para la LOX (d), existiendo una correlación positiva entre ambos parámetros. B) Tinción de Rojo Alizarín en anillos aórticos procedentes de ratones transgénicos que sobreexpresan la LOX específicamente en células musculares lisas (TgLOX) y animales normales (wild-type). Los anillos se expusieron ex vivo a un medio de cultivo normal (Basal) o a un medio osteogénico rico en fosfatos (HPM) durante 4 días. Escala: 100 µm.